
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Электролитическая диссоциация | Электролитическая диссоциация (далее Э) распад вещества на ионы при растворении. Э происходит вследствие взаимодействия растворенного вещества с растворителем; по данным спектроскопических методов, это взаимодействие носит в значительной мере характер (см. Сольватация). Наряду с сольватирующей способностью молекул растворителя определенную роль в Э играет также макроскопическое свойство растворителя — его диэлектрическая проницаемость.
Классическая теория Э была создана С. Аррениусом и В. Оствальдом в 80-х гг. 19 в. Она основана на предположении о неполной диссоциации растворенного вещества, характеризуемой степенью диссоциации а, т. е. долей распавшихся молекул электролита. Динамическое равновесие между недиссоциированными молекулами и ионами описывается действующих масс законом. Например, Э бинарного электролита КА выражается уравнением типа КА Û К+ + А-. Константа диссоциации Кд определяется активностями катионов аК+, анионов аА- и недиссоциированных молекул аКА следующим образом:
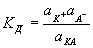 (1) (1)
Значение Кд зависит от природы растворенного вещества и растворителя, а также от температуры и может быть определено несколькими экспериментальными методами. Степень диссоциации ее может быть рассчитана при любой концентрации a электролита с помощью соотношения:
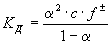 (2) (2)
где f± — средний коэффициент активности электролита (см. также Оствальда закон разбавления).
Классическая теория Э применима лишь к разбавленным растворам слабых электролитов. Сильные электролиты в разбавленных растворах диссоциированы практически полностью, поэтому представления о равновесии между ионами и недиссоциированными молекулами лишено смысла. Согласно представлениям, выдвинутым в 20—30-х гг. 20 в. В. К. Семенченко (СССР), Н. Бьеррумом (Дания), Р. М. Фуоссом (США) и др., в растворах сильных электролитов при средних и высоких концентрациях образуются ионные пары и более сложные агрегаты. Современные спектроскопические данные показывают, что ионная пара состоит из двух ионов противоположного знака, находящихся в контакте ("контактная ионная пара") или разделенных одной или несколькими молекулами растворителя ("разделенная ионная пара"). Ионные пары электрически нейтральны и не принимают участия в переносе электричества. В сравнительно разбавленных растворах сильных электролитов равновесие между отдельными сольватированными ионами и ионными парами может быть приближенно охарактеризовано, аналогично классической теории Э, константой диссоциации (или обратной величиной — константой ассоциации). Это позволяет использовать уравнение (2) для расчета соответствующей степени диссоциации, исходя из экспериментальных данных.
В простейших случаях (большие одноатомные однозарядные ионы) приближенные значения константы диссоциации в разбавленных растворах сильных электролитов можно вычислить теоретически, исходя из представлений о чисто электростатическом взаимодействии между ионами в непрерывной среде — растворителе.
Лит.: Измайлов Н. А., Электрохимия растворов, 3 изд., М.,1976; Monk . В., Electrclytic dissociation, L. — . ., 1961.
А. И. Мишустин. |
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |
|