
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Гесса закон | Гесса закон (далее Г), основной закон термохимии, согласно которому тепловой эффект реакции зависит лишь от начального и конечного состояний системы и не зависит от промежуточных состояний и путей перехода. Г был открыт Г. И. Гессом в 1840 на основе экспериментальных исследований. Он представляет собой одну из форм позднее открытого закона сохранения энергии в применении его к реакциям и относится к процессам, происходящим при постоянном объеме или при постоянном давлении. Г широко используется для определения расчетным путем теплового эффекта интересующего процесса на основе экспериментальных данных, относящихся к др. процессам (в т. ч. даже к процессам, практически недоступным в данных условиях). Так, для 298,15 К теплоту образования окиси (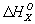 ккал/моль) из графита можно рассчитать, зная, что теплоты сгорания ккал/моль) из графита можно рассчитать, зная, что теплоты сгорания 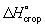 окиси и графита до 2 при этой температуре равны соответственно —282,99 и —393,32 кдж/моль (—67,635 и—94,051 ккал/моль). Рассматривая два пути образования 2 из графита при непосредственном сжигании его до 2 и при промежуточном образовании СО (см. рис.) и зная, что по Г общий тепловой эффект обоих путей перехода должен быть одинаковым, находим окиси и графита до 2 при этой температуре равны соответственно —282,99 и —393,32 кдж/моль (—67,635 и—94,051 ккал/моль). Рассматривая два пути образования 2 из графита при непосредственном сжигании его до 2 и при промежуточном образовании СО (см. рис.) и зная, что по Г общий тепловой эффект обоих путей перехода должен быть одинаковым, находим 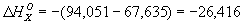 ккал/моль (теплота выделяется). ккал/моль (теплота выделяется).
В. А. Киреев.
|
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |
|