
|

|
Большая Советская Энциклопедия (цитаты)
|

|

|
 |
Энтальпия | Энтальпия (далее Э) (от греч. enthálpo - нагреваю) (теплосодержание, тепловая функция Гиббса), потенциал термодинамический, характеризующий состояние термодинамической системы при выборе в качестве основных независимых переменных энтропии и давления р. Обозначается (, р, , xl), где - число частиц системы, xi - другие макроскопические параметры системы. Э - аддитивная функция, т. е. Э всей системы равна сумме Э составляющих ее частей; с внутренней энергией системы Э связана соотношением
= + pV, (1)
где - объем системы. Полный дифференциал Э (при неизменных и xi) имеет вид:
dH = TdS + Vdp. (2)
Из формулы (2) можно определить температуру Т и объем системы:
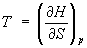 , , 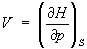 . .
При постоянном давлении (р = const.) теплоемкость системы
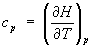
Эти свойства Э при р = const аналогичны свойствам при постоянном объеме:
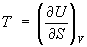 , , 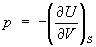 и и 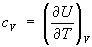 . .
Равновесному состоянию системы в условиях постоянства и р соответствует минимальное значение Э Изменение Э (DН) равно количеству теплоты, которое сообщают системе или отводят от нее при постоянном давлении, поэтому значения DН характеризуют тепловые эффекты фазовых переходов (плавления, кипения и т. д.), реакций и других процессов, протекающих при постоянном давлении. При тепловой изоляции тел (в условиях р = const) Э сохраняется, поэтому ее называют иногда теплосодержанием или тепловой функцией. Условие сохранения Э лежит, в частности, в основе теории Джоуля - Томсона эффекта, нашедшего важное практическое применение при сжижении газов. Термин "Э" был предложен Х. Камерлинг-Оннесом.
Д. Н. Зубарев. |
Для поиска, наберите искомое слово (или его часть) в поле поиска
|

|
 |
 |
 |

|

|
Новости 02.05.2026 17:53:02
|

|

|
 |
|

|
 |
 |
 |
|